Real-Time PCR快速反应液(染料法)是采用SYBR Green I嵌合荧光法进行Real-Time PCR的专用试剂,可对目标DNA进行快速、特异性的定量检测。优化的预混液可缩短Real-Time PCR的反应时间,适用于标准或快速PCR仪。
2×QuickFire SYBR qPCR Mix采用了抗体修饰的Anti Taq DNA聚合酶,配合独特的快速PCRBuffer体系可确保在所有的Real-Time PCR仪上进行灵敏的qPCR反应,具有反应快速、PCR反应时间缩短60%,同时具有高扩增效率,高扩增特异性和宽广的可信范围的特点,使你在不影响PCR效果的前提下更快获得结果,节约科研时间和能源。

- 2×QuickFire SYBR qPCR Mix采用了抗体修饰的Anti Taq DNA聚合酶,配合特制的快速PCR Buffer体系,可大大缩短变性、退火与延伸时间,可节省多达60%的反应时间,快速获得实验结果。
- 本制品特制的快速PCR Buffer体系含有独特的PCR稳定因子,在不损失PCR灵敏度和特异性的基础上进行快速反应,保证了2×QuickFire SYBR qPCR Mix高扩增效率,高扩增特异性和宽广的可信范围的特点。
- 2×QuickFire SYBR qPCR Mix中预混有SYBR Green I,PCR反应液配制时,只需加入模板、引物、灭菌蒸馏水便可进行快速Real-Time PCR反应,操作简单方便。
- 本制品附带ROX Reference Dye,用于消除信号本底以及校正孔与孔之间产生的荧光信号误差,方便客户针对不同型号荧光定量PCR仪时选择对应浓度使用。

本制品采用了特异的抗体修饰热启动DNA聚合酶进行快速PCR扩增,通过检测反应进程中SYBR Green I的荧光强度,达到检测PCR产物扩增量的目的,适用于标准和快速PCR仪。
- 本制品中特异的抗体修饰热启动DNA聚合酶,95℃条件下孵育1min即可激活全部酶活,在缩短变性时间的同时避免了非特异性产物的扩增。
- 本制品的快速PCR Buffer体系添加了独特的PCR稳定因子,配合精心优化的快速PCR Buffer体系,可大大缩短变性、退火和延伸时间,使PCR总运行时间缩短60%,更快获得实验结果,而不影响PCR反应效果。
- 本制品针对cDNA模板和gDNA模板结构组成的差异,对PCR的反应步骤进行了特别的优化,使较难扩增的gDNA模板也能获得良好的PCR结果。

| 组分 | 125T | 500T | 5000T |
| 2×QuickFire SYBR qPCR Mix | 1.25mL | 4×1.25mL | 40×1.25mL |
| 50×ROX Reference Dye | 250μL | 1mL | 10×1mL |
| RNase-Free ddH2O | 2×1mL | 5×1mL | 50×1mL |
保存:-20℃,避免反复冻融,有效期1年。

收到本制品后,请立即置于-30~-15℃避光保存。从-30~-15℃取出使用时,将冻存的QuickFire SYBR qPCR Mix和ROX Reference Dye融解,然后轻轻颠倒混匀,待溶液完全均一后再行使用。如解冻后没有使用,须彻底混匀后重新冷冻。(在解冻过程中盐会出现分层现象,未混匀进行冷冻,盐晶体的析出将会对酶造成损害)。如需一段时间内经常取用,可在2~8℃条件下储存3个月。避免反复多次冻融。

- 本制品中含有荧光染料SYBR Green I,保存本制品或配制PCR反应液时应避免强光照射。
- 如果试剂没有混匀,其反应性能会有所下降。使用时请上下颠倒轻轻混匀,请不要使用振荡器进行混匀,尽量避免出现泡沫,并经瞬时离心后使用。
- 引物纯度对反应特异性影响很大,建议使用PAGE级别以上纯化的引物。
- 引物终浓度为0.3μM可以在大多数体系中获得良好的扩增结果。如果需要进一步优化,可以在0.2~0.5μM范围内调整引物浓度。
- 20μL反应体系中,cDNA模板的使用量一般小于100ng,基因组DNA模板量一般小于50ng,逆转录产物作为模板时,使用量应不超过PCR体系终体积的20%。

- 建立Real-Time PCR反应体系
- 融解QuickFire SYBR qPCR Mix(如果保存在-20℃)、ROX Reference Dye、引物和RNase-Free ddH2O,并将所有试剂在室温下融解并彻底混匀。
- 建议置于冰上进行Real-Time PCR反应液的配制。
成分 50μL体系 25μL体系 20μL体系 终浓度 2×QuickFire SYBR qPCR Mix 25μL 12.5μL 10μL 1× 正向引物(10μM) 1.5μL 0.75μL 0.6μL 300 nM 反向引物(10μM) 1.5μL 0.75μL 0.6μL 300 nM cDNA模板 - - - -ng-pg 50×ROX Reference Dye - - - - RNase-Free ddH2O 至50μL 至25μL 至20μL - - 引物终浓度为300 nM可以在大多数体系中获得良好的扩增结果。扩增效率不高时,可增加PCR反应体系中的引物浓度;发生非特异扩增时,可适当减少PCR反应体系中的引物浓度。需要进一步优化引物浓度的,可以在200~500 nM范围内调整。
- 几种常见仪器的匹配ROX Reference Dye浓度见下表:
仪器 浓度 ABI PRISM 7000/7300/7700/7900HT/StepOne等 5×(例如5μL ROX/50μL体系) ABI 7500、7500 Fast;Stratagene Mx3000P、Mx3005P和Mx4000等 1×(例如1μL ROX/50μL体系) Roche仪器,Bio-Rad仪器,Eppendorf仪器等 无需添加
- 引物终浓度为300 nM可以在大多数体系中获得良好的扩增结果。扩增效率不高时,可增加PCR反应体系中的引物浓度;发生非特异扩增时,可适当减少PCR反应体系中的引物浓度。需要进一步优化引物浓度的,可以在200~500 nM范围内调整。
- 融解QuickFire SYBR qPCR Mix(如果保存在-20℃)、ROX Reference Dye、引物和RNase-Free ddH2O,并将所有试剂在室温下融解并彻底混匀。
- 进行Real-Time PCR反应
- 建议采用两步法PCR反应程序进行反应;若模板量较低等因素导致扩增效果不佳,可使用三步法程序进行PCR反应。
- 两步法反应程序:
阶段 循环 温度 时间 内容 荧光信号采集 预变性 1 95℃ 1min 预变性 否 PCR反应 40 95℃ 5sec 变性 否 60℃△1 15sec△2 退火/延伸 是 熔解曲线分析(Melting/Dissociation Curve Stage) - 三步法反应程序:
阶段 循环 温度 时间 内容 荧光信号采集 预变性 1 95℃ 1min 预变性 否 PCR反应 40 95℃ 5sec 变性 否 50~60℃△3 10sec 退火 否 72℃ 15sec△2 延伸 是 熔解曲线分析(Melting/Dissociation Curve Stage)
注△2:使用不同型号仪器进行时间设定时,请按照仪器使用说明书要求进行实验操作,几种常见仪器的时间设定见下表:
注△3:通常引物退火温度比引物的解链温度(Tm)低5℃,如果引物碱基数较少,可以适当提高退火温度,这样可以使PCR的特异性增加;如果碱基数较多,那么可以适当减低退火温度。使用ABI 7700/7900HT/7500 Fast,Roche,BioRad和Agilent等公司荧光定量PCR仪时请设定在15sec。 使用ABI 7000和7300时请设定在31sec。 使用ABI7500时请设定在32sec。 - 两步法反应程序:
- 盖上反应管,轻柔混匀。可短暂离心,确保所有组分均在管底。
- 将反应体系置于荧光定量PCR仪中,开始反应。
- 建议采用两步法PCR反应程序进行反应;若模板量较低等因素导致扩增效果不佳,可使用三步法程序进行PCR反应。

Real-Time PCR反应举例(PCR仪选用ABI 7500 Fast):
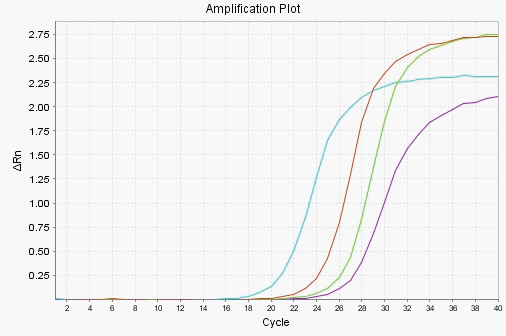 | 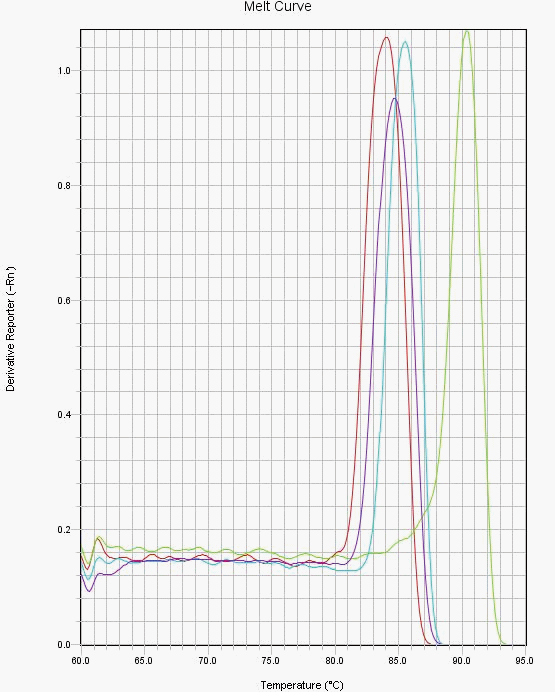 |
| 图1.扩增曲线,4对不同检测体系以单链cDNA为模板,利用2×QuickFire SYBR qPCR Mix | 图2.熔解曲线,经qPCR测试后,通过图2熔解曲线分析,均为单一峰,未发现非特异性扩增和引物二聚体产生。cDNA合成是使用反转录试剂盒进行。 |
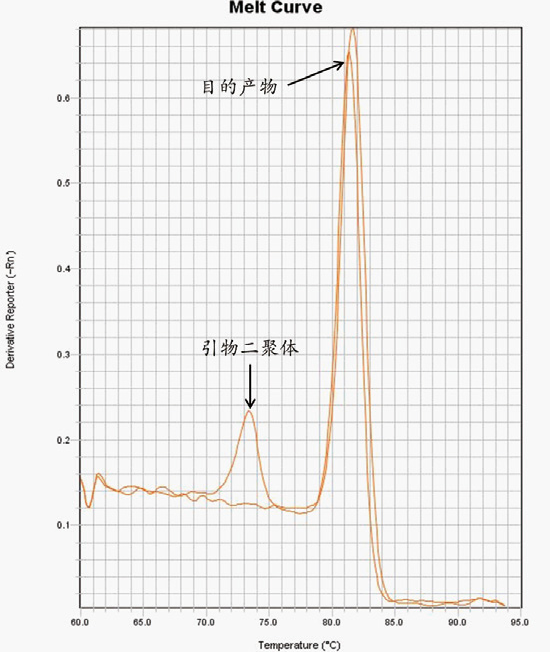 | |
| 图3.使用2×QuickFire SYBR qPCR Mix的熔解曲线仅有单一峰,为特异性扩增产物,其Tm值为83.5℃;使用国外A公司试剂除了特异性扩增产物外,还出现了引物二聚体。引物二聚体的Tm值一般在75℃左右。 |

进行RT-qPCR反应时的操作建议:
进行RT-PCR反应时,有三种cDNA第一链合成试剂盒可以选择,分别是反转录试剂盒,cDNA第一链合成反应预混液和cDNA第一链合成试剂盒。
反转录试剂盒可3min去除基因组DNA的残留,使基因定量结果更加真实可信,适用于模板量为50ng~2μg的总RNA的快速反转录(共需21min),是荧光定量PCR的反转录实验的优秀选择。
- 将模板RNA在冰上解冻;5×gDNA Buffer、FQ-RT Primer Mix、10×King RT Bu?er、RNase-Free ddH2O在室温(15~30℃)解冻,解冻后迅速置于冰上。使用前将每种溶液涡旋振荡混匀,简短离心以收集残留在管壁的液体。
- 以下操作步骤请在冰上进行。为了保证反应液配制的准确性,进行各项反应时,应先配制成Mix,然后再分装到每个反应管中。
- 按照表1的基因组DNA的去除体系配制混合液,彻底混匀。简短离心,并置于42℃,孵育3min。然后置于冰上放置。
表1.gDNA去除反应体系成分 用量 5×gDNA Buffer 2μL Total RNA - RNase-Free ddH2O 至10μL - 按照表2的反转录反应体系配制混合液。
表2.反转录反应体系成分 用量 10×King RT Buffer 2μL Quicking Enzyme Mix 1μL FQ-RT Primer Mix 2μL RNase-Free ddH2O 至10μL - 将反转录反应中的mix,加到gDNA去除步骤的反应液中,充分混匀。
- 42℃,孵育15min。
- 95℃,孵育3min之后放于冰上,得到的cDNA可用于后续荧光定量PCR反应或低温保存。

进行Real-Time PCR反应时,PCR引物的设计非常重要。设计PCR扩增效率高,反应特 异性强的引物可以参考以下要求。
| 引物长度 | 18~30个碱基 |
| GC含量 | 40~60% |
| Tm值 | 引物软件都可以给出Tm,与引物长度,碱基组成,引物使用缓冲的离子强度也有关。 上下游引物的Tm值要尽量接近。 简单的Tm计算公式为:Tm = 4℃(G + C)+ 2℃(A + T)。 一般采用较引物Tm值低5℃作为PCR退火温度。 提高退火温度可以增加PCR反应的特异性。 |
| 引物及PCR扩增产物序列 | PCR扩增产物适宜长度在80~200bp之间。 尽量避开在模板的二级结构区域设计引物。 避免上下游引物3′端之间形成2个或以上的互补碱基以减少引物二聚体的形成。 引物3'端碱基不能有多于3个连续的G或C。 引物自身不应存在互补序列,否则引物自身会折叠成发夹状结构。 避免引物3'末端碱基为T。 引物序列中A、T、G、C要尽量均匀分布。 |

- 无扩增信号或扩增曲线起峰晚或仅有引物二聚体
问题 分析 DNA模板中存在抑制剂 重新纯化模板或降低模板使用量 Mg2+浓度不合适 使用2×QuickFire SYBR qPCR Mix时,PCR反应体系中Mg2+的终浓度为2mM。对有些扩增体系,可以将Mg2+终浓度提高到5mM。进行Mg2+终浓度优化时,建议每次增加0.5mM Mg2+浓度进行实验。 加样错误或试剂问题 检查试剂浓度和保存条件,包括所使用的引物和模板。重复进行实验。 PCR条件、引物序列或浓度不当 请确认引物未发生降解,引物浓度及PCR条件,扩增不好时,通常先尝试降低退火温度,延长退火时间和提高引物浓度,有时也可以提高退火温度,增加延伸时间,降低升温速度。对于GC含量高的模板,可以适当延长变性时间。如果还是扩增不好,请重新设计引物。 起始模板问题 检查起始模板的浓度,保存条件和质量。重新对模板进行线性梯度稀释,并用新稀释模板进行实验。增加起始模板使用量。 - NTC出现较高的荧光值
问题 分析 试剂污染 建议使用新试剂进行实验。 PCR反应液配制时发生污染 采取必要的防污染策略(如使用带滤芯的枪头)。 引物出现降解 可以使用变性聚丙烯酰胺胶检测引物降解情况。 - 出现引物二聚体和(或)非特异扩增
问题 分析 Mg2+浓度不合适 使用2×QuickFire SYBR qPCR Mix的反应体系含有Mg2+的终浓度为2mM。对有些扩增体系,可以将Mg2+终浓度增加到5mM。建议每次增加0.5mM Mg2+浓度进行优化。 PCR退火温度太低 建议每次增加2℃进行退火温度优化。 引物设计不合适 考虑重新设计引物序列。 PCR产物太长 荧光定量PCR产物适宜长度在100~150bp之间,而且不应该超过500bp。 引物出现降解 可以使用变性聚丙烯酰胺胶检测引物降解情况。 计量误差 反应体积太小会导致检测精度下降。请根据定量PCR仪推荐的反应体积重新实验。 - 定量值重现性差
问题 分析 仪器方面的故障 因为仪器的不适用,在温度管理或检测时产生重现性差。请根据相应仪器的说明书进行点检。 样品纯度不好 不纯的样品会导致实验的重现性差。 稀释的模板放置太久 通过梯度稀释的模板最好现配现用。 引物质量下降 尽量避免新合成引物批次间的差异,可以使用原来质量好的引物做为对照。 PCR反应条件、引物浓度、序列等不恰当 扩增效率差的PCR较容易产生重现性差。通过变更引物的浓度或PCR反应条件来进行调整。扩增不好时,一般可降低退火温度或提高引物浓度,也可以延长延伸时间。如模板的GC含量较高,可延长变性时间。仍得不到改善时,建议重新设计引物。 计量误差 反应体积太小会导致检测精度下降。请根据定量PCR仪推荐的反应体积重新实验。
相关搜索:Real-Time PCR快速反应液(染料法),Real-Time PCR,qPCR预混液,qPCR预混反应液,qPCR反应预混液,嵌合荧光法,荧光定量PCR,qPCR Mix,qPCR扩增,染料法,SYBR Green I,快速PCR,2×QuickFire SYBR qPCR Mix



